Membrane et transport
Toute machine (moteurs thermiques, organismes vivants...) consiste fondamentalement à diminuer localement l'entropie au détriment d'un ensemble plus vaste. Cela suppose la division de l'espace en compartiments qui soient en partie perméables. Dans beaucoup de dispositifs (piles, batteries, cellules vivantes...), ce rôle est assuré par des membranes dont la porosité permet le transport maitrisé de molécules d'un compartiment à l'autre. Nous étudions expérimentalement ce transport transmembranaire d'un point de vue fondamental sur des membranes synthétiques (en polymère ou en alumine) ou mimant des membranes biologiques (bicouches lipidiques).
La science procède souvent par analogie. Ainsi, une catégorie de transport unidirectionnel moléculaire basé sur des mécanismes analogues à celui d'une roue à cliquet est devenue un objet d'étude en-soi de la physique statistique (cf. P. Hänggi, F. Marchesoni. Artificial brownian motors: Controlling transport on the nanoscale. Rev. Mod. Phys., 81:387, 2009). Ces mécanismes sont dits browniens s'ils fonctionnent grâce à l'agitation thermique, ce qui est paradoxal puisqu'ils tendent à diminuer l'entropie. Les deux exemples ci-dessous, pris dans des domaines très différents, relèvent de cette catégorie. D'un point de vue électrique, il s'agit de diode à courant ionique qui fonctionnent grâce à l'agitation thermique.
Pores coniques synthétiques
Le déplacement d'ions à travers une membrane pourvue de canaux (pores) résulte de forces qui s'exercent en général directement et individuellement sur les ions, comme par exemple celles provenant d'un champ électrique transmembranaire. Mais théoriquement, le bilan de ces forces fait également intervenir un terme d'une toute autre nature. En effet, lorsque le transit est suffisamment lent pour que les ions aient le temps d'explorer transversalement par mouvement brownien le canal, les variations longitudinales de sa section produisent un gradient d'entropie auquel correspond une force. Aussi lorsque le canal a une forme asymétrique (par exemple en entonnoir), cet effet peut induire un mécanisme anti-retour similaire à une roue à cliquet ou au clapet d'une pompe fonctionnant à un niveau moléculaire: les ions s'avancent dans le pore mais reviennent difficilement en arrière.
Pour vérifier cette idée, nous avons conçu et réalisé une expérience basée sur le principe suivant: cette force entropique dépend de la taille des ions, aussi lorsque celle-ci est très différente pour les anions et les cations, nous pouvons nous attendre à ce que des pores coniques redressent un courant ionique alternatif. C'est précisément ce que nous avons observé en réalisant des membranes par attaque chimique des traces laissées par une irradiation aux ions lourds et en utilisant une solution diluée de polyacide comme électrolyte.
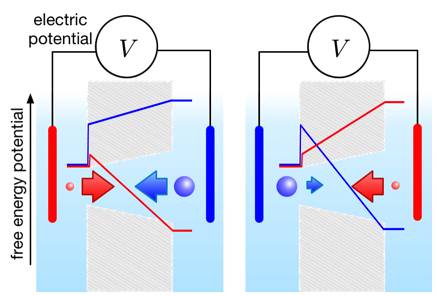
Schéma de principe d'une diode entropique basée sur la forme géométrique du canal.
Pour en savoir plus :
The concept of entropic rectifier facing experiments, Sci. Rep., 6: 38966, 2016
Pores peptidiques des membranes biologiques
L'interaction des membranes cellulaires avec les molécules adsorbées à leur surface et la façon dont l'incorporation de ces molécules s'opère sont encore mal comprises. Nous nous sommes intéressés aux peptides antimicrobiens qui sont à la base du système immunitaire inné des organismes pluricellulaires. Essentiellement, ces peptides rendent les membranes perméables en y formant des pores. Leur présence universelle, leur action non-spécifique et à large spectre ainsi que leur structure très élémentaire laissent entrevoir un mode d'action selon des mécanismes physiques eux aussi très généraux et universels.
Nous avons traité ce problème au moyen d'expériences dites de "tension imposée" (consistant à mesurer le courant ionique transmembranaire) et de réflectivité des neutrons. En particulier, nous avons montré que l'ouverture des pores présentent une dynamique lente et typique de la transition vitreuse, qui pourrait être gouvernée par les fluctuations en surface de la concentration des peptides telles qu'elles sont prévues par le modèle RSA (pour Random Sequential Adsorption). Plus récemment, nous nous sommes intéressés à la thermodynamique de l'ouverture des pores en fonction de la tension électrique transmembranaire et de la température. Nos résultats nous permettent de proposer un nouveau mécanisme physique où l'adsorption des peptides et le champ électrique tendent tous deux à courber la membrane et dans lequel le coût entropique de l'ouverture d'un pore provient d'un effet "d'aire exclue" pour la translation des lipides et explique comment la tension-seuil nécessaire varie avec la température.
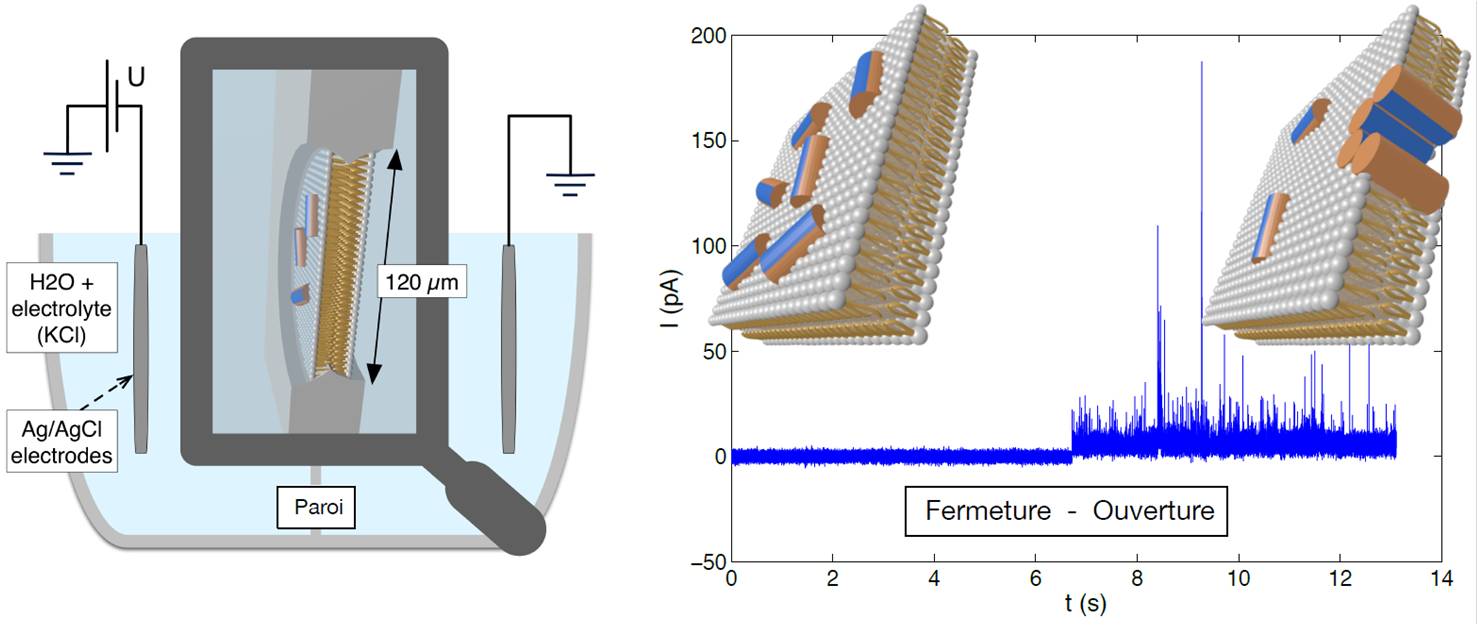
Une membrane autosupportée séparant deux électrolytes permet de détecter l'ouverture des pores : à ouvert/fermé correspond conducteur/isolant.
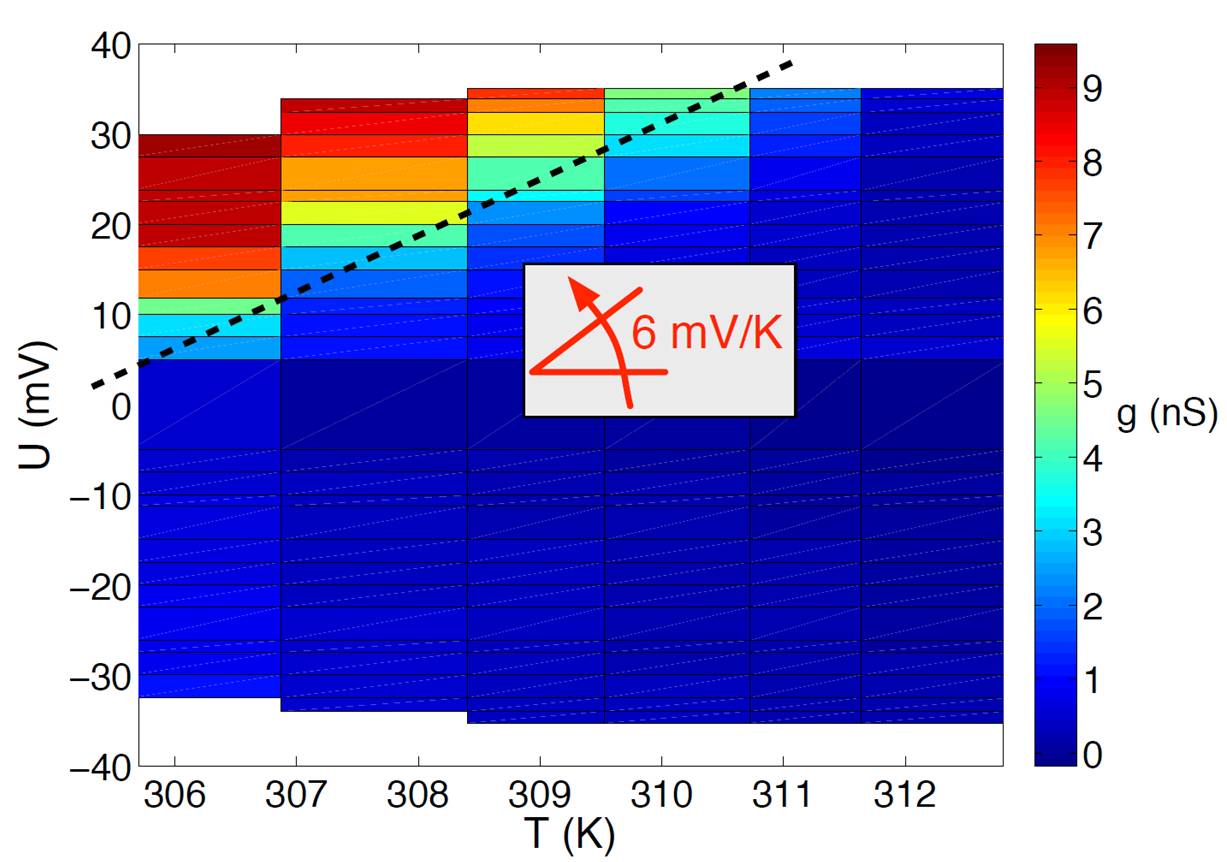
Conductance (g) d'une bicouche lipidique (DPPC) en présence du peptide alaméthicine en fonction du potentiel U du compartiment peptidique et de la température T. La ligne pointillée correspond à la transition.
Pour en savoir plus :
Peptide pores in lipid bilayers : voltage facilitation pleads for a revised model, Phys. Rev. Lett., 111: 028102, 2013
Fluctuations of ionic current through lipid bilayer at the onset of peptide attacks and pore formation, Phys. Rev. Lett., 103: 180601, 2009


