Dynamique structurale de la Guanylate Cyclase et de la NO-Synthase
Chercheurs :
Michel Negrerie
Jean-Louis Martin
Personnel Permanents :
Jean-Christophe Lambry
Isabelle Lamarre
Thésards :
Olga Petrova
Dynamique Structurale de la Guanylate Cyclase et de la NO-Synthase
Par spectroscopies résolues en temps (absorption et Raman) nous étudions les différents facteurs intervenant dans le contrôle de la dynamique du ligand diatomique NO par des hémoprotéines de la signalisation cellulaire. Toutes les propriétés de dynamique structurale de ces protéines sont mises en relation avec leurs propriétés biochimiques et physiologiques. Le NO, messager dans plusieurs voies de signalisation, est produit de façon endogène par la cellule et active des récepteurs spécifiques.
Nous étudions les mécanismes moléculaires de régulation, d'activation et de désactivation de la guanylate cyclase, le récepteur du NO endogène, de la NO-synthase endothéliale, produisant le NO dans les cellules, et de plusieurs senseurs bactériens du NO, homologues à la guanylate cyclase. Nous avons étendu ces études aux cytochromes c et c'.
Nos résultats montrent que la façon dont la structure protéique contrôle la dynamique du NO dans des échelles de temps picoseconde-nanoseconde différe selon la protéine, dépend étroitement de sa fonction et détermine sa réactivité. De plus, la dynamique du NO dépend de l'état allostérique de la protéine, modulé par la présence d'effecteurs liés à la protéine changeant son état d'activité. Les mesures spectroscopiques sont confrontées à des calculs de dynamique moléculaire.
Les changements de structure dans les récepteurs du NO et la NO-synthase sont identifiés par spectroscopie résolue en temps (0,1 picoseconde à 5 nanosecondes) et sont corrélés à l'état d'activation de la protéine (états allostériques) à la dynamique du NO et à l'affinité de la protéine pour le NO.
Techniques :
- Spectroscopie de résonance Raman résolue en temps (résolution temporelle 0,6 ps).
- Spectroscopie d'absorption transitoire (résolution temporelle 40 fs).
- Purification de protéines par FPLC et mesures d'activité catalytique
- Surexpression de guanylate cyclase dans le système cellules sf9 - baculovirus.
- Simulations de dynamique moléculaire.
Protéines étudiées :
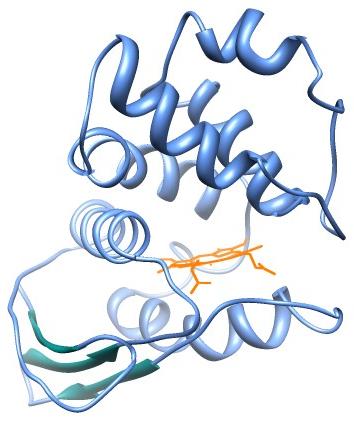
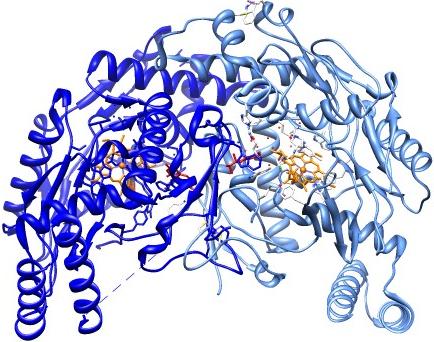
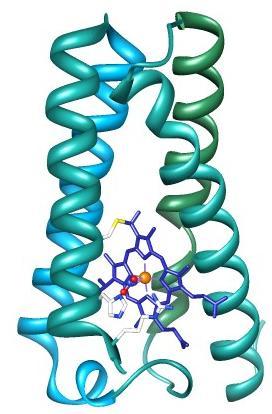

PBD file : 1XBN
Collaborations :
Dr Serguei Kruglik : spectroscopie Raman résolue en temps.
Laboratoire Acides Nucléiques et Biophotonique, Université Pierre & Marie Curie, Génopole Campus, 91030 Evry.
Dr Pierre Nioche : senseurs de NO homologues à la guanylate cyclase.
INSERM, UMR-S 747, Université Paris 5, France.
Pr Ah-Lim Tsai : NO-Synthase endothéliale.
Hematology and Internal Medicine, University of Texas Medical School, Houston, Texas, USA.
Pr Colin Andrew : cytochrome c'.
Biochemistry and Molecular Biology, Institut of Sciences and Technology, Beaverton, Oregon, USA.
Pr C.S. Raman : NO-sensors homologous to guanylate cyclase.
Biochemistry and Molecular Biology, University of Texas Medical School, Houston, Texas, USA.
Pr Stefan Franzen : déterminants structuraux de la dynamique du NO dans la myoglobine.
Department of Chemistry, North Carolina State University, Raleigh, NC 27695, USA.
Proposition de Thèse / Proposed PhD thesis subject :
"Dynamique structurale de la guanylate cyclase et de senseurs bactériens de l'oxyde nitrique (NO) étudiée par spectroscopie Raman résolue en temps".
La guanylate cyclase (GC) est le récepteur du NO endogène chez les mammifères et se trouve impliquée dans de nombreux processus physiologiques. En réponse à la fixation du NO, la GC convertit le GTP en GMP. Ses mécanismes d'activation et de désactivation sont inconnus. Cette hémoprotéine est constituée de deux sous-unités, dont l'une comporte le site de fixation du NO et l'autre le site catalytique (GTP à GMP). Nous cherchons déchiffrer les mécanismes moléculaires de son activation. Par spectroscopie Raman résolue en temps nous chercherons à identifier les intermédiaires structuraux induits par le relargage du NO et sa refixation. Ce travail de thèse comporte l'utilisation d'un spectromètre Raman (0,6 ps - 1,5 ns) existant au Laboratoire d'Optique et Biosciences (ainsi que des mesures de cinétiques d'aborption picoseconde) et l'analyse des spectres dans le cadre d'un modèle allostériques de la protéine. Ce sujet nécessite des connaissances en spectroscopie des protéines et une participation à la purification de protéines et de mesures biochimiques, essentiellement la mesure de l'activité catalytique de la GC par dosage immuno-enzymatique.
Selected publications :
N. Ben Brahim, N. Bel-Haj Mohamed, M. Poggi, R. Ben Chaâbane, M.Haouari, H. Ben Ouada, M. Negrerie.
Interaction of L-cysteine functionalized CdSe quantum dots with metallic cations and selective binding of cobalt in water probed by fluorescence.
(2017) Sens. Act. B 243, 489–499.
C. R. Andrew, O. N. Petrova, I. Lamarre, J.-C. Lambry, F. Rappaport and M. Negrerie.
The Dynamics Behind the Affinity: Controling Heme-Gas Affinity via Geminate Recombination and Heme Propionate Conformation in the NO-Carrier Cytochrome c'.
(2016) ACS Chem. Biol. 11, 3191–3201.
N. Ben Brahim, M. Poggi, N. Bel-Haj Mohamed, R. Ben Chaâbane, M. Haouari, M. Negrerie & H. Ben Ouada.
Synthesis, characterization and spectral temperature-dependence of thioglycerol-CdSe nanocrystals.
(2016) Journal of Luminescence 177, 402–408.
N. Ben Brahim, N. B. H. Mohamed, M. Echabaane, M. Haouari, R. Ben Chaâbane, M. Negrerie & H. Ben Ouada
Thioglycerol-functionalized CdSe quantum dots detecting cadmium ions.
(2015) Sens. Act. B 220, 1346–1353.
Yoo, B.-K., Lamarre, I., Martin, J.-L., Rappaport, F., & Negrerie, M.
Motion of proximal histidine and structural allosteric transition in soluble guanylate cyclase.
(2015) Proc. Natl. Acad. Sci. USA 112, E1697–E1704.
Ramos-Alvarez, C., Yoo, B.-K., Pietri, R., Lamarre, I., Martin, J.-L., Lopez-Garriga, J. & Negrerie, M.
Reactivity and dynamics of H2S, NO and O2 interacting with hemoglobins from Lucina pectinata.
(2013) Biochemistry 52, 7007–7021.
Yoo, B.-K., Lamarre, I., Martin, J.-L., Andrew, C. & Negrerie, M.
Picosecond binding of the His ligand to four-coordinate heme in cytochrome c': a one-way gate for releasing proximal NO.
(2013) J. Am. Chem. Soc. 135, 3248–3254.
Yoo, B.-K., Lamarre, I., Rappaport, F., Nioche, P., Raman, C.S., Martin, J.L. & Negrerie, M.
Picosecond to Second Dynamics Reveals a Structural Transition in Clostridium botulinum NO-Sensor Triggered by the Activator BAY-412272.
(2012) ACS Chem. Biol. 7, 2046–2054.
Yoo, B.-K., Kruglik, S. G., Lamarre, I., Martin, J.-L., & Negrerie, M.
Absorption Band III Kinetics Probe the Picosecond Heme Iron Motion Triggered by Nitric Oxide Binding to Hemoglobin and Myoglobin.
(2012) J. Phys. Chem. B. 116, 4106–4114.
Yoo, B.-K., Lamarre, I., Martin, J.-L., & Negrerie, M.
Quaternary structure controls ligand dynamics in soluble guanylate cyclase.
(2012) J. Biol. Chem. 287, 6851–6859.
Kruglik, S. G., Lambry, J.-C., Martin, J.-L., Vos, M. H. & Negrerie, M.
Sub-picosecond Raman spectrometer for time-resolved studies of structural dynamics in heme proteins.
(2011) J. Raman Spectrosc. 42, 265–275.
Kruglik, S. G., Yoo, B.-K., Franzen, S., Vos, M. H., Martin, J.-L. & Negrerie, M.
Picosecond primary structural transition of the heme is retarded after nitric oxide binding to heme proteins.
(2010) Proc. Natl. Acad. Sci. USA. 107, 13678-13783.
B.-K. Yoo, I. Lamarre, J.-L. Martin, C. R. Andrew, P. Nioche & M. Negrerie
Understanding the mechanism of nitric oxide sensors and receptors at molecular level"
in: EKC2008 Proceedings of the EU-Korea Conference on Science and Technology.
(2008) Springer Proceedings in Physics (Springer Berlin), Ed: Yoo, S. D. Vol. 124, 517-524
Download PDF
Sauviat, M.-P., Colas, A., Chauveau, M.-J., Drapier, J.-C. & Negrerie, M.
"Hypericin activates L-type Ca2+ channels in cardiac myocytes.
(2007) J. Nat. Prod. 70, 510-514.
Kruglik, S. G., Lambry, J.-C., Cianetti, S., Martin, J.-L. , Eady, R. R., Andrew, C. R. & Négrerie, M.
Molecular basis for nitric oxide dynamics and affinity with Alcaligenes xylosoxidans cytochrome c' .
(2007) J. Biol. Chem. 282, 5053-5062. Download PDF
M. Négrerie, S. G. Kruglik, J.-C. Lambry, M. H. Vos, J.-L. Martin & S. Franzen
Role of Heme Iron Coordination and Protein Structure in the Dynamics and Geminate Rebinding of Nitric Oxide to H93G Myoglobin : Implications for NO-Sensors.
(2006) J. Biol. Chem. 281, 10389-10398.
M. Négrerie, S. Cianetti, M. H. Vos, J.-L. Martin & S. G. Kruglik
Photoinduced coordination dynamics of cytochrome c: ferrous versus ferric species studied by time-resolved resonance Raman and transient absorption spectroscopies.
(2006) J. Phys. Chem. B. 110, 12766-12781. Download PDF
M. Négrerie, J.-L. Martin & H.-O. Nghiêm
Functionality of nitrated acetylcholine receptor : the two-step formation of nitrotyrosines reveals their differential role in agonist and neurotoxin binding.
(2005) FEBS Letters. 579, 2643-2647.
S. Cianetti, M. Négrerie, M. H. Vos, J.-L. Martin, & S.G. Kruglik,
Photodissociation of heme distal methionine in ferrous cytochrome c revealed by sub-picosecond time-resolved resonance Raman spectroscopy.
(2004) J. Am. Chem. Soc.126, 13932-13933.
Cianetti S., Kruglik, S.G., Vos, M.H., Turpin, P.-Y., Martin J.-L. & Négrerie, M.
Interaction of cytochrome c with NO studied by time-resolved raman and absorption spectroscopy.
(2004) Biochim. Biophys. Acta-Bionergetics 1658, 219 Suppl.
Proceedings of the 13th EBEC (2004 European BioEnergetics Conference) Pisa, Italy.
Gautier, C., Negrerie, M., Wang, Z.-Q., Lambry, J.-C., Stuehr, D. J., Collin, F., Martin, J.-L. & Slama-Schwok, A.
Dynamic Regulation of the Inducible Nitric-oxide Synthase by NO: comparaison with the endothelial isoform.
(2004) J. Biol. Chem. 279, 4358-4365. Download PDF
Liebl, U., Bouzhir-Sima, L., Kiger, L., Marden, M. C., Lambry, J.C., Negrerie, M. & Vos, M.H.
Ligand binding dynamics to the heme domain of the oxygen sensor Dos from Escherichia coli.
(2003) Biochemistry 42, 6527-6535.
Chowdhury, P., Gondry, M., Genet, R., Martin, J.L., Ménez, A., Negrerie, M. & Petrich J. W.
Picosecond dynamics of a peptide from the acetylcholine receptor interacting with a neurotoxin probed by tailored tryptophan fluorescence.
(2003) Photochem. Photobiol. 77, 151-157.
Liebl, U., Bouzhir-Sima, L., Negrerie, M., Martin, J.-L. & Vos, M.H.
Ultrafast ligand rebinding in the heme domain of the oxygen sensors FixL ans Dos : general regulatory implications for heme-based sensors.
(2002). Proc. Natl. Acad. Sci. USA. 99, 12771-12776.
Chirvony, V., Negrerie, M., Martin, J.-L. & Turpin, P.-Y.
Subpicosecond dynamics and mechanisms of quenching of photoexcited Cu(II)-porphyrin in solutions of Lewis bases.
(2002). J. Phys. Chem. 106, 5760-5767.
Slama-Schwok, A., Negrerie, M., Berka, V., Lambry, J.C., Tsai, A.L., Vos, M.H. & Martin, J.L.
Nitric oxide traffic in endothelial NO-synthase: evidence for a new NO binding site dependent on tetrahydrobiopterin?
(2002). J. Biol. Chem., 277, 7581-7586. Download PDF
Negrerie, M., Bouzhir, L., Martin, J.-L. & Liebl, U.
Control of nitric oxide dynamics by guanylate cyclase in its activated state.
(2001). J. Biol. Chem., 276, 46815-46821. Download PDF
Liebl, U, Lipowski, G., Negrerie, M., Lambry, J.-C., Martin, J.-L. & Vos, M.H.
Coherent reaction dynamics in a bacterial cytochrome c oxidase.
(1999) Nature 401, 181-184.
Négrerie, M., Berka, V., Vos, M.H., Liebl, U., Lambry, J.-C., Tsai, A-L., & Martin, J.-L.
Geminate recombination of nitric oxide to endothelial nitric oxide-synthase and mechanistic implications.
(1999) J. Biol. Chem. 274, 24694-24702. Download PDF
