Toxicité du sélénium
La sélénocystéine est un acide aminé nécessaire à l’activité de quelques enzymes anti-oxydantes importantes. À ce titre, le sélénium à l’état de traces, est un oligo-élément essentiel à la vie de nombreuses espèces, dont l’homme, À plus fortes doses, les composés du sélénium deviennent toxiques. Des études récentes suggèrent néanmoins qu’une administration de quantités supra-nutritionnelles de sélénium procure un bénéfice en s’attaquant préférentiellement aux cellules tumorales. La frontière reste cependant étroite entre les doses de sélénium toxiques et les doses prophylactiques ou thérapeutiques.
De nombreuses études sur divers systèmes modèles ont été réalisées pour définir les mécanismes à la base de la toxicité du sélénium ou de son rôle bénéfique dans la prévention du cancer. Il apparait que les différents composés séléniés ont des effets variables, dépendant de la forme chimique d’administration du métalloïde et des cellules sur lesquelles l’expérience est réalisée.
C’est dans ce contexte que nous nous sommes intéressés à l'importation, au stockage et à la toxicité de différents métabolites du sélénium chez la levure Saccharomyces cerevisiae. La levure est un modèle commode pour étudier la toxicité du sélénium. L’interconversion entre composés séléniés peut être contrôlée en utilisant des mutants génétiques, ce qui permet de suivre les voies métaboliques spécifiques de ces composés. En outre, cette levure n’incorpore pas de sélénocystéine dans ses protéines, ce qui écarte toute interférence de ces protéines dans nos études de toxicité.
Résultats récents
Mécanismes de la toxicité du séléniure d’hydrogène (Peyroche, G., Saveanu, C., Dauplais, M., Lazard., M, Beuneu, F., Decourty, L., Malabat, C., Jacquier, A., Blanquet, S. & Plateau, P., Sodium selenide toxicity is mediated by O2-dependent DNA breaks. PLoS One 7, e36343 (2012) [Abstract] [Full text])
Nos premiers travaux sur le sélénium, publiés en 2007, montrent que la toxicité de l’ion sélénite (SeO32-) pour la levure est nettement accrue par la présence de composés thiolés dans le milieu de culture, et que la production extracellulaire de séléniure d’hydrogène (H2Se) est à l’origine de cette hypertoxicité (Tarze et al., J. Biol. Chem. 282, 8759-8767 (2007)).
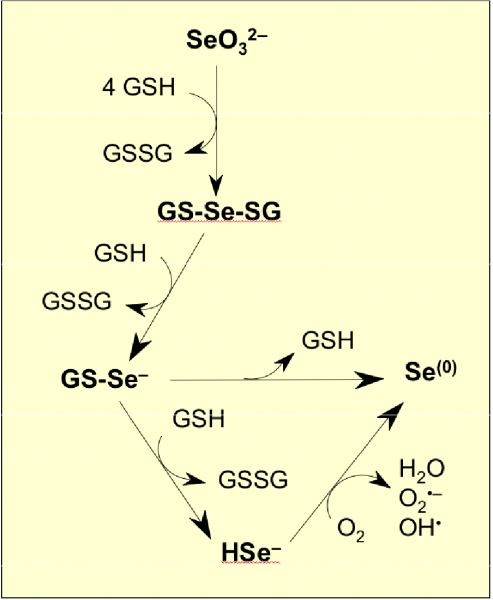
In vitro, le glutathione réagit spontanément avec le sélénite (SeO32-) pour former différents composés séléniés: sélénodiglutathion (GS-Se-SG), glutathiosélénol (GS-Se-), séléniure d’hydrogène (HSe-) and sélénium élémentaire (Se(0)).
Ce phénomène est à relier à l’observation selon laquelle des cellules cancéreuses résistantes aux traitements chimiothérapiques conventionnels deviennent remarquablement sensibles à la présence de sélénite. En effet, ces cellules chimio-résistantes exportent souvent davantage de cystéine que les cellules normales. Davantage de séléniure serait ainsi produit dans le voisinage des cellules malades, d’où une plus forte toxicité du sélénite vis-à-vis de ces cellules (Olm et al., Proc. Natl. Acad. Sci. USA 106, 11400-11405 (2009)).
Ces dernières années, le séléniure d’hydrogène (H2Se) est apparu comme un intermédiaire clé dans le métabolisme du sélénium. Nous avons cherché à identifier les causes de toxicité de ce composé. Pour cela, nous avons criblé une banque de mutants de délétion de levure (en collaboration avec l’unité de Génétique des interactions moléculaires de l'Institut Pasteur) et observé que, parmi les gènes dont l’absence cause une hypersensibilité à H2Se, on trouvait de nombreux gènes impliqués dans la recombinaison homologue ou dans les points de contrôle (checkpoints) des lésions dans l’ADN. Ce résultat suggère que les cassures double-brin de l'ADN sont une cause importante de la toxicité du séléniure. En accord avec cette hypothèse, l’incubation de cellules de levure avec du séléniure d'hydrogène entraîne une activation des points de contrôle de la transition G2/M et une fragmentation des chromosomes, comme nous avons pu le montrer par des expériences de FACS ou d’électrophorèse à champ pulsé.
Nous avons aussi constaté qu’in vitro, le séléniure d’hydrogène provoquait des cassures simple-brin dans l’ADN, à condition que du dioxygène (O2) soit présent. Or le séléniure d’hydrogène est connu pour réagir rapidement et spontanément avec le dioxygène pour former du sélénium élémentaire et de l’eau, mais surtout des dérivés réactifs de l’oxygène (ROS). Une inhibition de la formation des cassures dans l’ADN générées par le séléniure a été obtenue en présence de mannitol (un suppresseur des radicaux hydroxyle), mais pas en présence de superoxyde dismutase ou de catalase. En collaboration avec le Laboratoire des solides irradiés (LSI) de l’Ecole polytechnique, nous avons détecté par RPE, la signature caractéristique des radicaux •OH dans des solutions de séléniure d’hydrogène exposées au dioxygène. Enfin, conformément à ce que nos expériences in vitro suggèrent, nous avons montré que la toxicité du séléniure d’hydrogène pour la levure nécessitait bien la présence de dioxygène.
L’ensemble de ces résultats indique que la toxicité du séléniure d’hydrogène chez la levure découle de son oxydation par le dioxygène avec la production de radicaux libres qui provoquent des cassures dans l’ADN. On imagine que des cellules qui se divisent rapidement auront moins de temps que les autres pour réparer de telles cassures, ce qui pourrait expliquer une sensibilité particulière des cellules malignes au sélénium.

Puce à ADN (détail) utilisée pour identifier les gènes dont la délétion modifie la sensibilité au séléniure d’hydrogène. Rouge : plus sensible. Vert : moins sensible. Jaune : neutre.
Neutralisation par les métaux de la toxicité du séléniure de sodium (Dauplais, M., Lazard, M., Blanquet, S. & Plateau, P., Neutralization by metal ions of the toxicity of sodium selenide. PLoS One 8, e54353 (2013) [Abstract] [Full text])
Des granules inertes de séléniures métalliques ont été retrouvés dans les tissus de différents animaux sauvages. On pense qu’ils résultent de la présence concomitante des sels métalliques et de séléniure dans les cellules et qu’ils permettent une protection croisée vis-à-vis de la toxicité de ces métaux et du sélénium. Pour étudier systématiquement la toxicité de mélanges contenant un sel métallique et du séléniure, nous avons utilisé la mortalité de la levure Saccharomyces cerevisiae comme indicateur. En parallèle, nous avons évalué la capacité des ces mélanges à former des colloïdes. Les ions métalliques étudiés ont pu être rangés en trois catégories : (i) les métaux qui protègent les cellules de la toxicité du sélénium et forment un précipité colloïdal en présence de séléniure (Ag+, Cd2+, Cu2+, Hg2+, Pb2+ and Zn2+), (ii) ceux qui protègent les cellules en formant un précipité colloïdal insoluble et/ou en catalysant l’oxydation du séléniure d’hydrogène par le dioxygène (Co2+ and Ni2+), et enfin (iii), ceux qui ne protègent pas les cellules et n’interagissent pas (Ca2+, Mg2+, Mn2+) ou n’interagissent que faiblement (Fe2+) avec le séléniure.
Cette étude a souligné l’importance potentielle des métaux sur le statut en sélénium des individus. Comme on l’a mentionné ci-dessus, le sélénium administré en complément alimentaire pourrait diminuer l’émergence de certains cancers. À l’heure actuelle, cependant, les essais cliniques comparant l’incidence des cancers chez des patients ayant reçu ou non du sélénium restent vivement débattus. Ces essais peuvent être faussés par des variations non contrôlées de la biodisponibilité du sélénium d’un individu à l’autre. Clairement, des apports non contrôlés de métaux dans l’alimentation suivis de la formation de nanoparticules de séléniures métalliques pourraient contribuer à cette difficulté.
Transport du sélénodigluthathion par le transporteur vacuolaire Ycf1p de Saccharomyces cerevisiae (Lazard, M., Ha-Duong, N. T., Mounié, S., Perrin, R., Plateau, P. & Blanquet, S., Selenodiglutathione uptake by the Saccharomyces cerevisiae vacuolar ATP-binding cassette transporter Ycf1p. FEBS J. 278, 4112-4121 (2011) [Abstract])
Le transporteur vacuolaire Ycf1p de la levure Saccharomyces cerevisiae participe à la détoxification des métaux lourds en transportant vers la vacuole des adduits glutathion-métal. On pouvait s’attendre à un rôle positif d’Ycf1p dans la détoxification du sélénium. Or Pinson et al. ont montré que des mutants dépourvus d’Ycf1p étaient plus résistants au sélénite que la souche sauvage (Pinson et al. (2000), Identification of genes affecting selenite toxicity and resistance in Saccharomyces cerevisiae, Mol. Microbiol. 36, 679-687), et ont suggéré que le transport vers la vacuole de sélénite lié au glutathion pourrait conduire à un appauvrissement du cytoplasme en glutathion (GSH). Nous avons donc cherché à savoir si Ycf1p transportait le sélénodiglutathion (GS-Se-SG). Pour cela, nous avons synthétisé du sélénodiglutathion radioactif et préparé des vésicules de sécrétion contenant Ycf1p. Nos résultats montrent que le sélénodiglutathion est un substrat à forte affinité d’Ycf1p. Nous avons aussi mesuré le rapport GSH/GSSG dans des cellules exposées au sélénite exprimant Ycf1p, et montré qu’il était 6 fois plus faible que dans une souche dépourvue d’Ycf1p. Tous ces résultats indiquent que le transport de l’adduit sélénodiglutathion par Ycf1p diminue la concentration cytoplasmique de GSH, un processus qui, à son tour, peut augmenter la vulnérabilité des cellules au stress oxydant induit par le sélénite.
Importation du sélénite par les transporteurs de phosphate (Lazard, M., Blanquet, S., Fisicaro, P., Labarraque, G. & Plateau, P., Uptake of selenite by Saccharomyces cerevisiae involves the high and low affinity orthophosphate transporters. J. Biol. Chem. 285, 32029-32037 (2010) [Abstract] [Full text])
Alors que la toxicité du sélénite a été intensivement étudiée, on connaît encore mal le mécanisme par lequel ce composé traverse les membranes cellulaires. A pH physiologique, l’ion sélénite possède une taille et une charge similaire à celle de l’ion phosphate. De plus, une compétition entre le transport du sélénite et celui du phosphate a été observée dans des racines de blé. Nous nous sommes donc demandé si le sélénite et le phosphate n’utilisaient pas les mêmes transporteurs pour pénétrer dans la levure Saccharomyces cerevisiae.
Il existe 5 transporteurs de phosphate dans cette levure. Trois d’entre eux sont exprimés constitutivement et transportent le phosphate avec une faible affinité. Les deux autres, qui ont une forte affinité pour le phosphate, voient leur expression accrue lors d’une carence en phosphate. En utilisant des souches inactivées pour un ou plusieurs de ces transporteurs, nous avons montré que les transporteurs à faible et à forte affinité étaient impliqués dans l’importation du sélénite, et qu’il y avait une compétition entre le phosphate et le sélénite pour ces systèmes de transport du phosphate. Une inhibition par le phosphate de l’importation du sélénite ayant déjà été observée chez les plantes, chez l’algue verte Chlamydomonas reinhardtii et chez la levure Candida albicans, il semble que le transport opportuniste du sélénite par les transporteurs de phosphate soit un mécanisme général, au moins chez les plantes, les algues et les champignons.
Perspectives
Actuellement, nos travaux portent sur les mécanismes de la toxicité des séléno-métabolites organiques comme la sélénométhionine et la sélénocystéine, fréquemment utilisés dans les compléments alimentaires administrés à l’homme et aux animaux. Ces acides aminés sont-ils transformés en un intermédiaire métabolique commun, tel qu’H2Se, ou exercent-ils leur toxicité via des processus spécifiques non encore identifiés ?
Personnel
Permanents :
Myriam Lazard, Chargée de recherche au CNRS
Marc Dauplais, Ingénieur de recherche au CNRS
Sylvain Blanquet, Directeur de recherche émérite au CNRS et Professeur émérite à l’Ecole polytechnique
Pierre Plateau, Directeur de recherche au CNRS
Précédents membres du groupe
Chercheurs post-doctoraux :
Nguyet-Thanh Ha-Duong, chargée de travaux pratiques – Ecole polytechnique
Gérald Peyroche, PRAG – Ecole normale supérieure de Cachan
Romary Perrin, chargé de travaux pratiques – Ecole polytechnique
Agathe Tarze, boursière – Programme ToxNuc
Etudiants en thèse ou en master :
Ioana Grigoras
Stéphanie Mounié


